Publikacja zespołu z Pracowni Immunologii Doświadczalnej i Translacyjnej w prestiżowym Journal of Extracellular Vesicles
Z przyjemnością zawiadamiamy, że artykuł pt.: „Excess filaggrin in keratinocytes is removed by extracellular vesicles to prevent premature death and this mechanism can be hijacked by Staphylococcus aureus in a TLR2-dependent fashion” (doi: 10.1002/jev2.12335) został opublikowany w prestiżowym czasopiśmie naukowym Journal of Extracellular Vesicles, którego współczynnik wpływu (Impact factor) wynosi 17.337 oraz posiada maksymalną ocenę 200 punktów według Ministerstwa Edukacji i Nauki.
Autorem korespondencyjnym publikacji jest kierowniczka Pracowni Immunologii Doświadczalnej i Translacyjnej dr hab. Danuta Gutowska-Owsiak, prof. UG, a pierwszym autorem jest doktorant, mgr Adrian Kobiela. Współautorami są również obecni i byli członkowie laboratorium, dr Lilit Hovhannisyan, mgr Paulina Jurkowska, mgr Argho Aninda Paul, mgr Kinga Panek i dr Ewa Czechowska. W badaniach uczestniczyli ponadto dr hab. inż. Aleksandra Królicka, prof. UG (Zakład Badania Związków Biologicznie Czynnych), dr Michał Rychłowski (Zakładu Biologii Molekularnej Wirusów) oraz dr Aleksandra Bogucka (Laboratorium Spektrometrii Mas Zespołu Laboratoriów Specjalistycznych). Praca powstała przy współpracy z University of Oxford, Karolinska Institutet i Imperial College London oraz Gdańskim Uniwersytetem Medycznym.
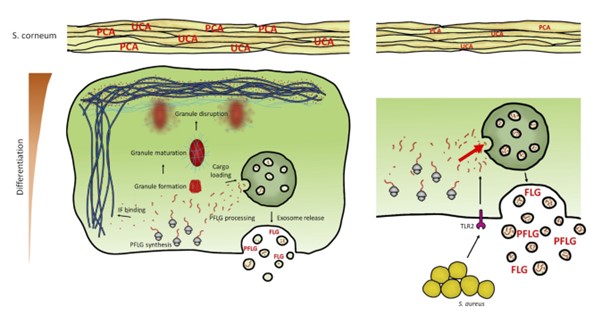
Skóra pacjentów cierpiących na przewlekłą chorobę zapalną skóry, atopowe zapalenie skóry (AZS) charakteryzuje się obniżonym poziomem białka filagryny. Profilagryna (PFLG) jest białkiem produkowanym głównie przez mocno zróżnicowane keratynocyty i jest niezbędna do utrzymania poprawnej funkcji bariery naskórkowej, m.in. wzmacniając ją mechanicznie i zapewniając przeciwbakteryjne działanie poprzez swoje produkty rozpadu. W górnych warstwach naskórka PFLG ulega proteolizie do aktywnych monomerów filagryny (FLG), które wiążą włókna keratynowe tworzące cytoszkielet tych komórek. W wyniku tego procesu keratynocyty obumierają tworząc warstwę rogową naskórka, co warunkuje nieprzepuszczalność wierzchniej warstwy skóry i skuteczną ochronę przed działaniem szkodliwych czynników środowiskowych.
Przy wzmożonej ekspresji w górnych warstwach naskórka, PFLG tworzy ziarna keratohialiny (KHG), które umożliwiają przestrzenną izolację tego białka w cytoplazmie, chroniąc komórki przed przedwczesną śmiercią. Natomiast do tej pory nie było wiadomo, w jaki sposób dochodzi do ekspresji tego białka w pozostałej części naskórka, i jak kontrolowana jest zawartość filagryny w jego głębszych, słabo zróżnicowanych warstwach, przed powstaniem KHGs. W naszej pracy pokazaliśmy, że PFLG/FLG obecne są już w warstwach naskórka zawierających słabo zróżnicowane keratynocyty, ale jej ilość jest zbyt mała do uformowania KHG, co mogłoby narażać komórki na przedwczesną śmierć. Nasza praca ukazała, że wydzielania tego białka za pomocą małych sekrecyjnych pęcherzyków zewnątrzkomórkowych (sEVs) stanowi mechanizm kontroli poziomu PFLG/FLG w cytoplazmie, dzięki czemu możliwe jest zapobieganie przedwczesnej śmierci komórek w najgłębszych warstwach naskórka, zanim poziom białka umożliwi powstanie ziarnistości.
Nasze badania pokazują, że sEVs krwi obwodowej zdrowych dawców, jak i pacjentów z AZS zawierają PFLG/FLG, co oznacza, że białko może być transportowane ze skóry do krwiobiegu. Co więcej, udokumentowaliśmy również zwiększenie wydzielania przez keratynocyty tych pęcherzyków ładowania do nich FLG przez gronkowca złocistego (Staphylococcus aureus), bakterię często kolonizującą pacjentów z AZS i wpływającą na stan ich skóry. W pracy wykazaliśmy, że procesy te są wynikiem aktywacji w keratynocytach receptora TLR2 rozpoznającego m.in. gronkowca. Przypuszczamy, że ten mechanizm może być wykorzystywany przez S. aureus jako ochronę przed przeciwdrobnoustrojowym działaniem produktów rozkładu FLG uwalnianej z keratynocytów uszkadzanych w wyniku infekcji.





